Projekt: C08
Dysregulation der Eisenhomöostase-induzierten zellulären inflammatorischen und neurodegenerativen Prozesse beim Glaukom
Das Glaukom ist weltweit die zweithäufigste Ursache für irreversible Erblindung und ist durch einen fortschreitenden Verlust retinaler Ganglienzellen (RGC) gekennzeichnet. Obwohl ein erhöhter intraokularer Druck (IOP) ein bekannter Risikofaktor ist und die IOP-Senkung eine etablierte Therapie darstellt, kann der Verlust der RGC trotz ausreichender Drucksenkung fortschreiten. Dies deutet darauf hin, dass ein einmal initiierter Teufelskreis unabhängig von der Kontrolle des IOP aufrechterhalten wird.
Wir und andere konnten zeigen, dass das Glaukom mit einer ausgeprägten Neuroinflammation und einer Aktivierung von Mikroglia einhergeht. Die zentrale Hypothese dieses Förderantrags ist, dass eine Wechselwirkung zwischen Glaukom und Neuroinflammation besteht, die unter anderem durch ein Ungleichgewicht der Eisenhomöostase ausgelöst wird. Das Eisenungleichgewicht ist die wahrscheinlichste Ursache für die Aktivierung ursprünglich ruhender Mikroglia. Daher schreitet die Glaukomerkrankung infolge der aktivierten Mikroglia weiter fort, obwohl der intraokulare Druck behandelt wird.
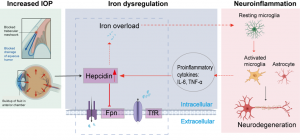
Das erste Ziel besteht darin, die Abfolge von IOP-Erhöhung und Neuroinflammation durch eine IOP-induzierte Hepcidin-Eisen-Dysregulation weiter zu untersuchen. Besonderes Augenmerk liegt dabei auf der Mikroglia-Aktivierung, der Sekretion proinflammatorischer Zytokine sowie auf Ferroptose infolge von Eisenüberladung und erhöhtem IOP in in-vivo-Modellen, Retina-Explantaten und Zellkulturexperimenten.
Das zweite Ziel besteht darin, diese Erkenntnisse in den humanen Kontext zu übertragen, indem Kammerwasser, Serum, Retina- und Sehnervgewebe von Glaukompatientinnen und -patienten analysiert werden.
Das dritte Ziel ist die Definition der pathophysiologischen Signalmechanismen des Glaukoms anhand von in-vivo– und in-vitro-Modellen mit genetischer Defizienz der BMP-Typ-I-Rezeptoren Alk2 und Alk3, die durch einen Schutz vor der Induktion inflammatorischer Parameter oder von Hepcidin gekennzeichnet sind, und diese Modelle einem erhöhten intraokularen Druck auszusetzen.
Zentrale Methoden:
• In-vivo-Glaukommodelle mit IOP-Erhöhung und genetisch veränderten Mäusen
• Retina-Explantatkulturen
• Mikroglia-spezifische Zellkulturmodelle
• Eisenüberladungs- und Ferroptose-Assays
• ELISA-basierte Zytokin- und Hepcidin-Analysen
• qPCR-gestützte Genexpressionsanalysen
• Immunhistochemische / immunfluoreszenzbasierte Proteinanalysen
• Analysen oxidativen Stresses und ROS-Messungen
• Untersuchung des Hepcidin–Ferroportin- und BMP-Signalwegs
• Translationale Analysen humaner Proben (Kammerwasser, Serum, Retina, Sehnerv)


