Projekt: C07
NLRP3-Inflammasom als therapeutisches Ziel bei atrophischer altersbedingter Makuladegeneration
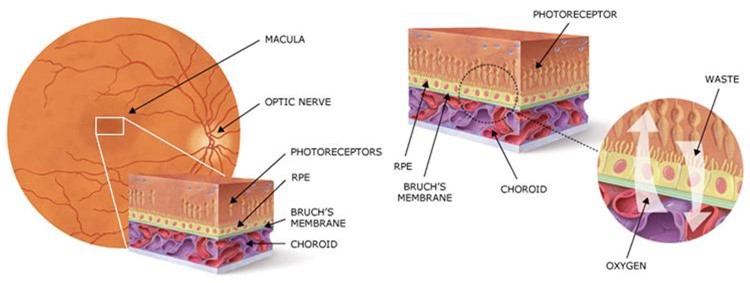
Die altersbedingte Makuladegeneration (AMD) ist die häufigste Ursache für irreversible Erblindung in Industrieländern. Für das erblindende, atrophische Spätstadium der Erkrankung fehlen bislang effektive Therapieoptionen, sodass ein hoher medizinischer Bedarf an neuen Behandlungsmöglichkeiten besteht. Zu den Schlüsselfaktoren in der Entwicklung und dem Fortschreiten der AMD zählen die Anhäufung von oxidativem und photooxidativem Schaden im retinalen Pigmentepithel (RPE), die fortschreitende Lipofuszin-Ablagerung im RPE sowie die chronische Aktivierung des angeborenen Immunsystems in der äußeren Netzhaut.
Ein zentraler Regulator des angeborenen Immunsystems ist der sogenannte Inflammasom-Komplex, ein intrazellulärer Sensor für vielfältige zelluläre Gefahrensignale. Inflammasome kontrollieren die Ausschüttung hochentzündlicher Zytokine wie IL-1β und IL-18. Insbesondere die Aktivierung des NLRP3-Inflammasoms (NACHT-, LRR- und PYD-Domänen-haltiges Protein 3) konnte im RPE und in der Netzhaut von Patient*innen mit atrophischer AMD nachgewiesen werden.
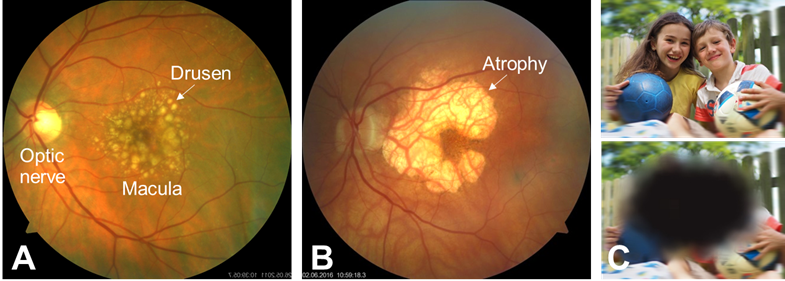
Wir haben die Mechanismen der Wechselwirkungen zwischen den oben genannten Faktoren der AMD-Pathogenese untersucht. Dabei konnten wir zeigen, dass lipofuszinvermittelte photooxidative Schäden an lysosomalen Membranen eine Aktivierung des NLRP3-Inflammasoms im retinalen Pigmentepithel (RPE) auslösen können, die zur Entstehung der AMD beitragen könnte. Zudem konnten wir eine Kommunikation des NLRP3-Signalwegs im RPE mit retinalen Mikrogliazellen und dem Komplementsystem nachweisen und die Mechanismen des RPE-Zelltods infolge der Inflammasom-Aktivierung charakterisieren.
In diesem Projekt möchten wir die Rolle der Inflammasom-Aktivierung bei der atrophischen AMD weiter aufklären und immunmodulatorische Behandlungsstrategien entwickeln. Dazu untersuchen wir die durch lipofuszinvermittelte photooxidative Schäden ausgelöste Aktivierung des NLRP3-Inflammasoms im RPE mithilfe neuartiger in vivo-Mausmodelle sowie ex vivo-Netzhautgewebekulturen der AMD. Ziel ist es, die zugrunde liegenden molekularen Mechanismen und betroffenen Zelltypen der Netzhaut zu identifizieren und die Wirksamkeit selektiver NLRP3-Inhibitoren zur Hemmung dieser Prozesse zu testen – als Grundlage für die Entwicklung von Inflammasom-Inhibitoren als potenzielle Therapieoption bei atrophischer AMD.